| "Descrizione" by A_Partyns (12948 pt) | 2023-Apr-13 19:34 |
Review Consensus: 10 Rating: 10 Number of users: 1
| Evaluation | N. Experts | Evaluation | N. Experts |
|---|---|---|---|
| 1 | 6 | ||
| 2 | 7 | ||
| 3 | 8 | ||
| 4 | 9 | ||
| 5 | 10 |
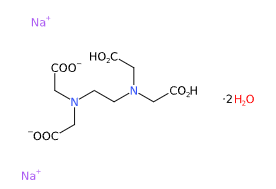
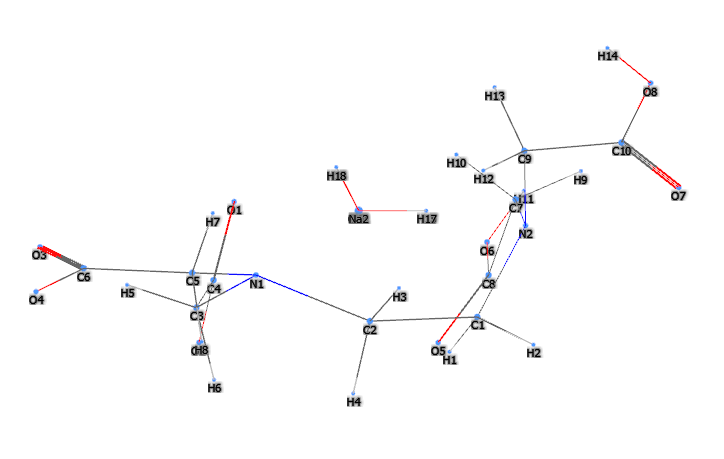
E385 o Disodium EDTA (Ethylenediaminetetraacetic acid disodium salt) è un composto chimico, sale disodico de EDTA, chelante di ioni di calcio e, tra i sali EDTA, il più importante.
Si presenta in forma di polvere bianca, inodore, insapore, facilmente solubile in acqua, ammoniaca, soluzioni acquose di idrossido di sodio, carbonato di sodio, difficilmente solubile in solventi organici come l'etere etilico o l'alcol.

A cosa serve e dove si usa
In chimica è un agente di complessazione a sei atomi di coordinazione che regola l'equilibrio tra ligando e ioni metallici, sovente addizionato al lisato a ioni complessi di magnesio e calcio per stabilizzare l'acido nucleico e degradare l'attività della nucleasi. Controlla la velocità di polimerizzazione. Ha inoltre funzione di agente chelante cioè un agente che si lega ad un altro per favorirne l'eliminazione o le reazioni dannose causate da ioni metallici e per formare un complesso stabile solubile in acqua. Questi studi ne spiegano il meccanismo (1). Può chelare con una grande maggioranza di ioni metallici diversi dai metalli alcalini quali calcio, magnesio, ferro, rame e altri ioni polivalenti.
Funziona anche come decalcificante (2) e come metodo antiossidante chiamato anche metodo Fenton (3).
Ampiamente utilizzato per prevenire l'ossidazione causata da metalli.
Alimentazione
Etichettato con il numero E385 nella lista degli additivi alimentari europei, il Disodium EDTA è un composto chimico che viene aggiunto agli alimenti con funzione di agente conservante e agente chelante per impedire il deterioramento del prodotto in cui è inserito e contrastare altri ingredienti.
Si trova in bevande gassate, gelatine, fagioli in scatola, maionese ed altro.
Per controllarne la presenza negli alimenti è stato sviluppato un metodo di rilevamento per la determinazione quantitativa : È stato sviluppato un metodo HPLC conveniente per la determinazione quantitativa dell'EDTA negli alimenti. L'EDTA nei campioni di cibo è stato facilmente estratto con acqua mediante ultrasuoni. Dopo la conversione in complesso Fe (III) in presenza di ioni Fe (III), l'EDTA è stata separata su una colonna C30 a fase inversa e rilevata con rivelazione ultravioletta (260 nm). Citrato e malato, che sono presenti in molti alimenti, formavano anche complessi Fe (III) ma non interferivano con la rilevazione cromatografica dell'EDTA. Il metodo consentiva la determinazione dell'EDTA negli alimenti a concentrazioni fino a 0,01 mmol / kg. Buoni recuperi (95,2-101%) sono stati ottenuti con il metodo di aggiunta standard su quattro campioni con elevata ripetibilità (RSD, 0,8-3,4%). Il metodo è stato applicato con successo all'analisi dell'EDTA in bevande gassate, gelatine, fagioli in scatola, mais in scatola e integratori alimentari (4).
Il Disodium EDTA è un noto miglioratore dell'assorbimento del ferro, tutta via i risultati di questo studio suggeriscono che in presenza di EDTA l'assorbimento del ferro avviene principalmente dal paracellulare anziché dal modo cellulare regolato, il che potrebbe potenzialmente aumentare la sua tossicità (5).
Per questo additivo alimentare è prevista una ADI (Acceptable Daily Intake) o GDA (Dose Giornaliera Ammissibile) massima di 2,5 grammi per Kg corporeo (6).
Cosmetica
Funziona come agente chelante e regolatore di pH nelle formulazioni cosmetiche. E' noto che questo agente chelante è citotossico e debolmente genotossico, ma non cancerogeno come conferma la relazione finale del gruppo di esperti per la revisione degli ingredienti cosmetici (7).
Agente chelante. Ha la funzione di evitare reazioni instabili e migliorare la biodisponibilità di componenti chimici all'interno di un prodotto, elimina i cationi di calcio e magnesio che possono causare una velatura nei liquidi limpidi.
Agente di controllo della viscosità. Controlla e adatta la viscosità al livello richiesto per ottenere una stabilità ottimale chimica e fisica del prodotto e del dosaggio in gel, sospensioni, emulsioni, soluzioni.
Medicina
Disodium EDTA è utilizzato in forma di somministrazione endovenosa nella terapia chelante per l'avvelenamento da piombo e metalli pesanti, nel trattamento della tendinite calcificata, come anticoagulante e battericida per il suo basso costo.
Altri usi
- additivo, sbiancante e fissante per la lavorazione di materiali fotosensibili a colori
- depuratore e detergente per l'acqua
- prodotti chimici agricoli
- inibitore per la crescita delle piante
- placcatura chimica, galvanica senza cianuro
Per approfondire:
Caratteristiche tipiche del prodotto commerciale Ethylenediaminetetraacetic acid disodium salt
| Appearance | White powder |
| pH | 4.0-5.0 |
| Boiling Point | >100°C 614.2°C at 760 mmHg |
| Melting Point | 248°C |
| Flash Point | 325.2ºC |
| Density | 1.01 g/mL at 25°C |
| Vapor Pressure | 1.15E-16mmHg at 25°C |
| Chlorides | 0.01% Max |
| Sulphates | 0.1% Max |
| Iron | 0.001% Max |
| Heavy metal | 0.001% Max |
| Chelating value | 221 |
| NTA | 0.2% |
| Water insoluble matter | ≤0.005% |
| Loss on drying | 8.7- 11.4% |
| Aminotriacetic acid | ≤10 ppm |
| Storage | 2-8°C |
| Chemical Risk |  |
 |  |
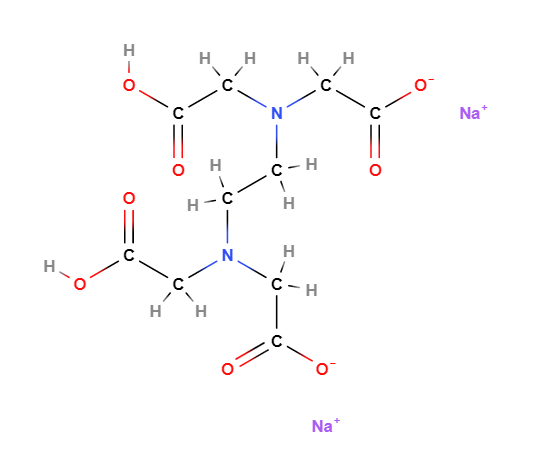 |  |
- Molecular Formula C10H18N2Na2O10 C10H14N2O8Na2.2H2O
- Linear Formula [-CH2N(CH2CO2Na)CH2CO2H]2
- Molecular Weight 336.21
- Exact Mass 336.054565
- CAS 139-33-3 6831-92-6 (Ethylenediaminetetraacetic acid disodium salt dihydrate)
- UNII
- EC Number 205-358-3
- DSSTox Substance ID DTXSID9027073
- IUPAC disodium;2-[2-[carboxylatomethyl(carboxymethyl)amino]ethyl-(carboxymethyl)amino]acetate
- InChl=1S/C10H16N2O8.2Na/c13-7(14)3-11(4-8(15)16)1-2-12(5-9(17)18)6-10(19)20;;/h1-6H2,(H,13,14)(H,15,16)(H,17,18)(H,19,20);;/q;2*+1/p-2
- InChl Key ZGTMUACCHSMWAC-UHFFFAOYSA-L
- SMILES C(CN(CC(=O)O)CC(=O)[O-])N(CC(=O)O)CC(=O)[O-].[Na+].[Na+]
- MDL number MFCD00070672
- PubChem Substance ID 329747771
- RTECS AH4410000
- NCI C65508
- FEMA 4520
- HS Code 2922499990
- Beilstein 3822669
- eCl@ss 39030907
- NACRES NA.25
Sinonimi :
Ethylenediaminetetraacetic acid, Disodium salt, Disodic EDTA, Disodic edetate, Acid Edetic
Bibliografia_____________________________________________________________________
(1) Retrievability of calcium hydroxide intracanal medicament with three calcium chelators, ethylenediaminetetraacetic acid, citric acid, and chitosan from root canals: An in vitro cone beam computed tomography volumetric analysis.
Raghu R, Pradeep G, Shetty A, Gautham PM, Puneetha PG, Reddy TVS.
J Conserv Dent. 2017 Jan-Feb;20(1):25-29. doi: 10.4103/0972-0707.209068.
Comparison of efficiency of ethylenediaminetetraacetic acid, citric acid, and etidronate in the removal of calcium hydroxide intracanal medicament using scanning electron microscopic analysis: An in-vitro study.
Chockattu SJ, Deepak BS, Goud KM.
J Conserv Dent. 2017 Jan-Feb;20(1):6-11. doi: 10.4103/0972-0707.209079.
(2) An in vitro study on the efficacy of removing calcium hydroxide from curved root canal systems in root canal therapy.
Wang Y, Guo LY, Fang HZ, Zou WL, Yang YM, Gao Y, Yang H, Hu T.
Int J Oral Sci. 2017 Jun;9(2):110-116. doi: 10.1038/ijos.2017.14. Epub 2017 Jun 23.
(3) Cosmeceutical Effects of Galactomannan Fraction from Arenga pinnata Fruits In vitro.
Yanti, Madriena, Ali S.
Pharmacognosy Res. 2017 Jan-Mar;9(1):39-45. doi: 10.4103/0974-8490.199773.
Effect of Selected Plant Phenolics on Fe2+-EDTA-H₂O₂ System Mediated Deoxyribose Oxidation: Molecular Structure-Derived Relationships of Anti- and Pro-Oxidant Actions.
de Graft-Johnson J, Nowak D.
Molecules. 2016 Dec 31;22(1). pii: E59. doi: 10.3390/molecules22010059.
(4) Determination of ethylenediaminetetraacetic acid in foods by reversed-phase high-performance liquid chromatography.
Kemmei T, Kodama S, Yamamoto A, Inoue Y, Hayakawa K.
Food Chem. 2013 Jun 1;138(2-3):866-9. doi: 10.1016/j.foodchem.2012.11.103. Epub 2012 Dec 5.
(5) Interactions between ethylenediaminetetraacetic acid (EDTA) and iron absorption pathways, in the Caco-2 model.
Kibangou IB, Bureau F, Allouche S, Arhan P, Bouglé D.
Food Chem Toxicol. 2008 Nov;46(11):3414-6. doi: 10.1016/j.fct.2008.08.014. Epub 2008 Aug 20.
(6) http://www.fao.org/ag/agn/jecfa-additives/specs/Monograph1/Additive-164.pdf
(7) Lanigan RS, Yamarik TA. Final report on the safety assessment of EDTA, calcium disodium EDTA, diammonium EDTA, dipotassium EDTA, disodium EDTA, TEA-EDTA, tetrasodium EDTA, tripotassium EDTA, trisodium EDTA, HEDTA, and trisodium HEDTA. Int J Toxicol. 2002;21 Suppl 2:95-142. doi: 10.1080/10915810290096522.
| Evaluate |

